درمان بیماریهای چشمی و سلولهای بنیادی

سلولهای بنیادی ، درمان نوین بیماریهای چشمی
تحقیقات اخیر حاکی از این است که پیوند سلولهای بنیادی یک درمان بالقوه برای بیماریهای تحلیلبرنده شبکیه ای ارائه میدهد که در حال حاضر درمان مؤثری برای آنها وجود ندارد. این بیماریها شامل تحلیلبرندههای ارثی شبکیه و تحلیل برنده ماکولای وابسته به سن (AMD) هستند که هر دو میتوانند منجر به کاهش شدید بینایی یا نابینایی شوند. در درمان های مبتنی بر سلول ها بینادی، چشم از اهمیت زیادی برخوردار است. زیرا چشم، و بهویژه شبکیه، به دلایل متعددی هدف ایدهآلی برای درمانهای جایگزینی سلولی است. اول اینکه محل پیوند و سلولها را میتوان مستقیماً از طریق معاینات بالینی و دستگاههای تصویربرداری با وضوح بالا از شبکیه بررسی کرد. همچنین، معیارهای بالینی متعددی برای اندازهگیری عملکرد بینایی وجود دارد، از جمله حدت بینایی، حساسیت کنتراست، میکروپریمتر، الکتروفیزیولوژی و تطابق در تاریکی. دوم اینکه اندازه کوچک بافتهای داخل چشمی اجازه میدهد تا از حجمهای کوچکتر و تعداد کمتری از سلولهای جایگزین نسبت به سایر اعضای بدن استفاده شود. سوم اینکه دسترسی جراحی به چشم و شبکیه امکان تزریق سلولها بهصورت معلق یا بهصورت ورقههایی بر روی مواد داربستی که میتواند به بقای سلولهای پیوندی کمک کند، فراهم میکند. در نهایت، برخلاف سایر ساختارهای سیستم عصبی مرکزی، شبکیه دارای لایهای غیر سیناپسی بهنام اپیتلیوم رنگدانهای شبکیه (RPE) است که ممکن است نسبت به سلولهای فتورسپتور یا سلولهای گانگلیونی شبکیه که به اتصالات سیناپسی با سلولهای مجاور نیاز دارند، پذیرای بیشتری برای پیوند سلولی باشد.
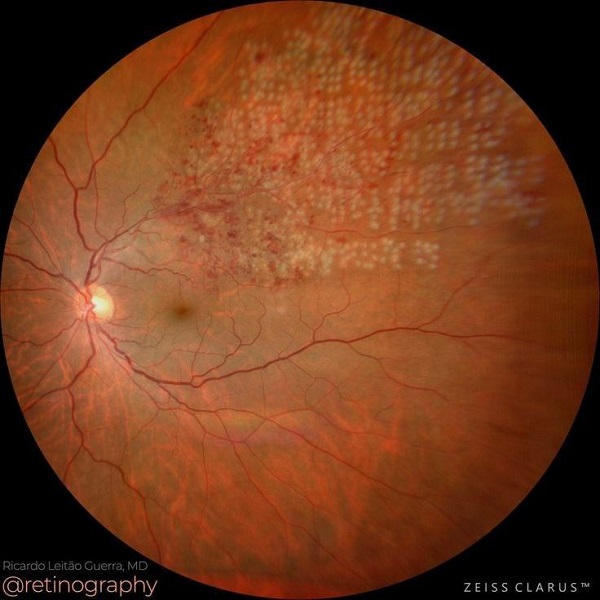
استراتژیهای درمانی سلولهای بنیادی برای درمان بیماریهای چشمی
درمانهای مبتنی بر سلولهای بنیادی بهعنوان درمانهای بالقوه یا حتی شاید درمان قطعی برای چندین نوع دژنراسیون شبکیه که در حال حاضر غیرقابل درمان هستند، در نظر گرفته میشوند .دو رویکرد متمایز از درمانهای مبتنی بر سلولهای بنیادی در حال توسعه هستند:
استراتژی دوزدهی موقت در درمان بیماریهای پشمی
این رویکرد شامل استفاده از سلولهای بنیادی چندتوان یا سلولهای پیشساز چشمی است که به صورت غیرقطبی تزریق میشوند. این سلولها عوامل محافظ عصبی و تعدیلکننده ایمنی غیرانتخابی را فراهم میکنند که اثر درمانی آنها تا زمانی که سلولهای پیوندی زنده و قادر به ترشح این عوامل باشند، ادامه دارد. این ایده براساس تحقیقات قبلی که از عوامل نوروتروفیک مانند فاکتور نوروتروفیک مژک (CNTF) برای حفاظت از سلولهای شبکیه استفاده میکردند، شکل گرفته است.
- مطالعات و نتایج قبلی
اثرگذاری عوامل نوروتروفیک: مطالعات نشان دادهاند که CNTF و عوامل دیگر مانند فاکتور نوروتروفیک مشتق از گلیا (GDNF)، میتوانند گیرندههای نوری را در مدلهای حیوانی تحلیل شبکیه حفاظت کنند.
- آزمایشات بالینی
در آزمایشات بالینی فاز I و II، CNTF برای بیماریهایی مانند رتینیت پیگمنتوزا (RP)، تلانژکتازی ماکولا نوع ۲ تست شده است. اگرچه CNTF به عنوان ایمن شناخته شده است، اما نتایج نشان نداد که این درمان در بهبود حدت بینایی یا حساسیت میدان دید در بلندمدت (تا ۹۶ ماه) مزیت دارد.
- بررسی سلولهای بنیادی
فرضیه جدید: با بررسی بیشتر سلول های بنیادی پژوهشگران یافتند که دامنه وسیعتری از عوامل
نوروتروفیک ترشح شده توسط سلولهای بنیادی ممکن است موثرتر باشد.
- آزمایشات سلولهای بنیادی
در ادامه برای اثبات فرضیه بالا، انواع مختلف سلولهای بنیادی، از جمله سلولهای بنیادی مشتق شده از بند ناف و سلولهای بنیادی عصبی مشتق شده از مغز جنین، در آزمایشات فاز I و II برای dAMD تست شدهاند. اگرچه این آزمایشات به عنوان ایمن شناخته شدند، اما به دلیل عدم موفقیت و عدم سازگاری این سلولها با منشأ چشمی متوقف شدهاند.
- تلاشهای جاری
تلاشهای اخیر بر روی سلولهای بنیادی پیشساز شبکیه از چشمهای جنینی انسانی متمرکز شدهاند. شرکتهای JCyte و Reneuron در حال انجام آزمایشات بالینی برای تست تزریق داخل زجاجیه و زیر شبکیه این سلولها برای درمان انواع موروثی RP هستند.
- مکانیسم درمانی
سلولهای پیشساز شبکیه ممکن است مکانیسم درمانی خاصتری نسبت به سایر سلولهای بنیادی داشته باشند که میتواند منجر به بازسازی واقعی گیرندههای نوری شود. با این حال، تمایز ناپیوسته این سلولها به انواع مختلف سلولهای شبکیه نگرانیهایی را درباره یکنواختی اثرات درمانی و پاسخ ایمنی ایجاد میکند.
استراتژی کاشت دائمی
این روش از سلولهای مشتق از سلولهای بنیادی پرتوان استفاده میکند که سلولهای گیرنده نوری شبکیه و یا سلولهای اپیتلیوم رنگدانهای شبکیه (RPE) را هدف قرار میدهند. هدف این است که همان نوع سلولهایی که تحلیل رفتهاند، جایگزین شوند.
در تلاشهای علمی برای درمان بیماریهای چشمی مانند رتیننت پیگمنتوزا (RP) و دژنراسیون ماکولا وابسته به سن (AMD)، استراتژی کاشت دائمی با هدف جایگزینی بافت آسیبدیده یا تحلیلرفته شبکیه بهویژه مورد توجه قرار گرفته است.
این روش مشابه حمایت تغذیهای پیوندهای سلولهای بنیادی معلق است، اما با هدف اصلی بازگرداندن عملکردهای از دسترفته بافت شبکیه در مراحل پیشرفته بیماری. مطالعات بالینی نشان دادهاند که در مواردی که جراحی جابجایی RPE-کوروئید موفقیتآمیز بوده است، بینایی بیماران برای چندین سال تثبیت شده است. این امر نشاندهنده این است که پیوند RPE میتواند بهطور بالقوه درمانی مؤثر برایAMD باشد.
پیشرفتهای اخیر در تکنیکهای جراحی برای پیوندهای RPE و روشهای تمایز سلولهای RPE از سلولهای بنیادی، این پیوندها را برای بیماران AMD قابل انجام کرده است. از ابتدا، سلولهای رنگدانهدار از سلولهای بنیادی جنینی (ESCs) جدا شدهاند و محققان پروتکلهایی برای تولید سلولهای RPE بالغ از سلولهای بنیادی پرتوان القایی (iPSCs) و ESCs توسعه دادهاند. این پروتکلها با تقلید از فرآیند توسعه طبیعی جنینی، تبدیل سلولهای بنیادی به سلولهای RPE بالغ را تسهیل میکنند.
با توجه به رویکردهای مختلف در حال بررسی برای توسعه پیوندهای RPE، انتظار میرود آزمایشهای در حال انجام، اثربخشی پیوندهای RPE مشتق شده از منابع مختلف سلولهای بنیادی را در آینده نزدیک ارزیابی کنند.
چالشها و آیندهنگری
مانند هر روش درمانی جدیدی، درمان با سلول های بنیادی نیز محققان را با چالش هایی روبه رو می کند، که در ادامه به آن ها اشاره می شود:
- چالشهای تمایز و پاسخ ایمنی: تمایز ناپیوسته سلولهای پیشساز شبکیه چالشهایی را ایجاد میکند، زیرا اثرات درمانی ممکن است در بیماران متفاوت باشد. همچنین، سلولهای شبکیه تمایز یافته از این سلولها ممکن است با مشکلات نظارت ایمنی مواجه شوند.
- نیاز به تحقیقات بیشتر: پژوهشگران بر این باورند که برای بهینهسازی پنجره درمانی و درک اثربخشی سلولهای پیشساز شبکیه ، نیاز به مطالعات بیشتری است. در صورت موفقیت، این سلولها میتوانند یک درمان آماده برای انواع مختلف بیماریهای تحلیلبرنده شبکیه ارائه دهند.
گردآورنده: منا ابن التراب






دیدگاهتان را بنویسید