درمان ژنی ATSN-101 برای بهبود نابینایی ارثی
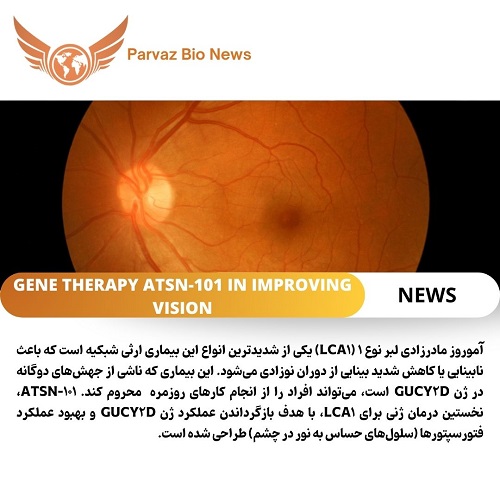
درمان ژنی ATSN-101، که برای بیماران مبتلا به آموروز مادرزادی لبر نوع ۱ (LCA1) توسعه یافته است، در یک مطالعه بالینی فاز ۱/۲ نتایج موفقیتآمیزی را در زمینه بهبود بینایی بیماران نشان داده است. آموروز مادرزادی لبر نوع ۱ (LCA1) یکی از شدیدترین انواع این بیماری ارثی شبکیه است که باعث نابینایی یا کاهش شدید بینایی از دوران نوزادی میشود. این بیماری که ناشی از جهشهای دوگانه در ژن GUCY2D است، میتواند افراد را از انجام کارهای روزمره مانند خواندن، رانندگی و حرکت در محیط محروم کند. ATSN-101، نخستین درمان ژنی برای LCA1، با هدف بازگرداندن عملکرد ژن GUCY2D و بهبود عملکرد فتورسپتورها (سلولهای حساس به نور در چشم) طراحی شده است.
طرح و هدف مطالعه
این مطالعه فاز ۱/۲ با هدف ارزیابی ایمنی و اثربخشی ژندرمانی ATSN-101 در بیماران مبتلا به LCA1 انجام شد. در این مطالعه ۱۵ بیمار با جهشهای تأیید شده ژن GUCY2D شرکت کردند که بین سالهای ۲۰۱۹ و ۲۰۲۲ از دو مرکز دانشگاهی در ایالات متحده، شامل دانشگاه پنسیلوانیا و دانشگاه علوم پزشکی اورگان، برای درمان ثبتنام شدند.
مطالعه به دو بخش تقسیم شد: در بخش اول که شامل بیماران بزرگسال بود، سه دوز مختلف ATSN-101 به صورت تزریق زیرشبکیهای به بیماران داده شد. در این بخش سه گروه از بیماران با دوزهای کم ۱.۰ × ۱۰¹⁰ vg/eye، متوسط ۳ × ۱۰¹⁰ vg/eye، و بالا۱ × ۱۰¹¹ vg/eye درمان شدند. پس از مشاهده نتایج ایمنی، در بخش دوم مطالعه (بخش توسعه دوز)، یک گروه بزرگسال و یک گروه کودک، همگی با بالاترین دوز مورد درمان قرار گرفتند. همه بیماران فقط در یک چشم تحت درمان قرار گرفتند تا تأثیرات و ایمنی این درمان بهتر ارزیابی شود.
ایمنی و عوارض جانبی درمان ژنی ATSN-101
در طی دوره مطالعه ۱۲ ماهه، عوارض جانبی متعددی مشاهده شد، اما اکثر آنها مربوط به جراحی بود و ارتباط مستقیمی با خود ژندرمانی نداشت. از ۶۸ عارضه جانبی ثبت شده، ۵۶ مورد به عمل جراحی مرتبط بود و تنها چند مورد التهاب چشمی خفیف ناشی از ژندرمانی گزارش شد که به خوبی با استفاده از استروئیدها کنترل گردید. التهاب چشمی که در برخی از بیماران مشاهده شد، عمدتاً خفیف و برگشتپذیر بود و با قطع درمان استروئیدی بهبود یافت. هیچ عارضه جدی یا بلند مدتی که مستقیماً به درمان ATSN-101 مرتبط باشد، ثبت نشد.
اثربخشی و بهبود عملکرد درمان ژنی ATSN-101 برای بینایی
نتایج اثربخشی این مطالعه بسیار امیدوارکننده بود، به ویژه در بیمارانی که بالاترین دوز درمانی را دریافت کردند. یکی از معیارهای اصلی برای ارزیابی بهبود بینایی، آزمایش حساسیت شبکیه در برابر نور (FST) بود. بیماران دریافتکننده دوز بالا در مدت ۱۲ ماه پس از درمان به طور میانگین ۲۰.۳ دسیبل (dB) بهبود در حساسیت نوری در چشم درمانشده نشان دادند، در حالی که چشمهای درماننشده تنها ۱.۱ دسیبل بهبود داشتند. این بهبودها بهسرعت و از ۲۸ روز پس از درمان مشاهده شد و در طول ۱۲ ماه ماندگار بود.
یکی دیگر از معیارهای اثربخشی، آزمون حرکتی چندنوری (MLMT) بود که برای ارزیابی توانایی بیماران در حرکت در محیطهای نوری مختلف طراحی شده است. در میان بیماران دریافتکننده دوز بالا، سه نفر از شش بیمار موفق شدند بالاترین نمره ممکن در آزمون حرکتی را کسب کنند. این نتایج نشان میدهد که این بیماران نه تنها حساسیت نوری بالاتری داشتند، بلکه توانستند توانایی خود را برای حرکت در محیطهای مختلف بهبود بخشند.
از نظر بینایی کلی، تغییرات در وضوح بینایی (BCVA) نیز مورد بررسی قرار گرفت. بیماران دریافتکننده دوز بالا به طور میانگین ۰.۱۶- لاگمار (logMAR) بهبود در چشم درمانشده خود تجربه کردند که معادل خواندن هشت حرف بیشتر در نمودار استاندارد بینایی است. هرچند این بهبود بهطور میانگین در مقایسه با بهبودهایی که در حساسیت نوری مشاهده شد کمتر بود، اما همچنان نشاندهنده بهبود واقعی در توانایی بیماران برای دیدن بهتر بود.
اهمیت نتایج و چشمانداز آینده
این مطالعه یکی از اولین آزمایشهای ژندرمانی برای بیماران مبتلا به LCA1 است که نشان میدهد این روش نه تنها ایمن است، بلکه میتواند به بهبود چشمگیر بینایی در بیماران کمک کند. نتایج امیدوارکننده در بیماران دریافتکننده دوز بالا، زمینهساز انجام آزمایشهای بالینی فاز ۳ برای ارزیابی اثربخشی بیشتر این درمان خواهد بود.
از آنجا که LCA1 یک بیماری نادر است و تاکنون هیچ درمان تأیید شدهای برای آن وجود نداشته، این ژندرمانی میتواند یک تحول بزرگ در زندگی بیماران ایجاد کند. بهبودهای قابل ملاحظه در حساسیت شبکیه نشان میدهد که ATSN-101 میتواند به عنوان یک درمان مؤثر و پایدار در نظر گرفته شود.
یکی از جنبههای کلیدی این مطالعه، حفظ بهبودهای حاصل در طول ۱۲ ماه بود. حتی در بیمارانی که بیش از ۱۲ ماه تحت نظر بودند، نتایج نشاندهنده پایداری اثرات درمان بود. این نشان میدهد که یک تزریق زیرشبکیهای از ATSN-101 میتواند اثرات طولانیمدت و پایداری بر بهبود بینایی داشته باشد.
چالشها و محدودیتها درمان ژنی ATSN-101
هرچند نتایج این مطالعه بسیار امیدوارکننده است، اما محدودیتهایی نیز وجود دارد. یکی از چالشهای اصلی در این مطالعه، اندازه کوچک نمونه بود که به دلیل نادر بودن بیماری LCA1 اجتنابناپذیر است. همچنین، این مطالعه به صورت برچسبباز (open-label) انجام شد، به این معنی که بیماران میدانستند کدام چشم درمان شده است، که ممکن است بر برخی از نتایج تأثیر گذاشته باشد. با این حال، بهبودهای مشاهده شده در آزمونهای عینی مانند FST و MLMT نشاندهنده بهبود واقعی در عملکرد بینایی بیماران بود.
همچنین، اگرچه بهبودهای قابل توجهی در حساسیت نوری در شرایط کمنور مشاهده شد، اما در شرایط نوری روشنتر بهبودهای مشابهی ثبت نشد. این امر ممکن است به دلیل تفاوت در پاسخهای فتورسپتورها به نور روشن و تاریک باشد. همچنین، بهبودهای وضوح بینایی (BCVA) کمتر از حد انتظار بود و نیاز به تحقیقات بیشتر در این زمینه وجود دارد.
نتیجهگیری
ATSN-101 به عنوان یک درمان ژنی برای بیماران مبتلا به LCA1، نتایج بسیار امیدوارکنندهای از نظر ایمنی و اثربخشی نشان داده است. این مطالعه نشان میدهد که این درمان میتواند به بهبود قابل توجهی در حساسیت شبکیه و عملکرد بینایی بیماران کمک کند. با توجه به این نتایج، ژندرمانی ATSN-101 بهعنوان یک گزینه بالقوه برای درمان LCA1 در آینده مطرح است و میتواند امید تازهای برای بیماران مبتلا به این بیماری نادر فراهم کند.
پیشبینی میشود که نتایج این مطالعه زمینهساز انجام آزمایشهای بالینی بزرگتر و با کنترل بیشتر در آینده شود تا اثربخشی این درمان به صورت دقیقتر ارزیابی گردد. با توجه به نبود درمانهای تأییدشده برای LCA1، ATSN-101 میتواند به عنوان اولین درمان برای این بیماری مطرح شود و به بیماران کمک کند تا کیفیت زندگی بهتری را تجربه کنند.
گردآرونده: منا ابن التراب
منبع:
Yang P, Pardon LP, Ho AC, Lauer AK, Yoon D, Boye SE, Boye SL, Roman AJ, Wu V, Garafalo AV, Sumaroka A. Safety and efficacy of ATSN-101 in patients with Leber congenital amaurosis caused by biallelic mutations in GUCY2D: a phase 1/2, multicentre, open-label, unilateral dose escalation study. The Lancet. 2024 Sep 7;404(10456):962-70.







دیدگاهتان را بنویسید